植物を使った感染症の研究
植物ウイルスの簡易検出法の開発と細胞間移行メカニズムの解明
ヒトと同様に植物も病気に感染し、作物の減収が起きることから、これらを検出・診断することは農業上重要です。石川助教らは、島根県のイチジク圃場に発生した原因不明の病気が、イチジクモザイクウイルス (FMV)という国内で未確認のウイルスによるものであることを突き止めました。FMVは世界的に見ても診断方法の確立されていないウイルスであったため、専門設備がなくても簡易迅速に感染を診断することのできる方法を開発しました。この診断法はキット化され「イチジクモザイク病診断キット」としてニッポン・ジーン社から販売されています。
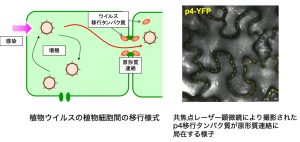
FMVは宿主への感染メカニズムがほとんど不明なウイルスであったため、その解明に取り組みました。特に侵入した細胞から隣接細胞に広がるメカニズムに着目して研究を行いました。FMVのゲノムにコードされるp4タンパク質が細胞間をつなぐチャネルである原形質連絡に局在し、ウイルスの細胞間移行を促進するウイルス移行タンパク質であることを示しました。さらに、p4移行タンパク質は、小胞体-細胞膜接着部位を形成すると考えられている植物タンパク質、シナプトタグミン1(SYT1)を利用して原形質連絡に侵入し、原形質連絡の機能を改変してウイルスの細胞間移行を促進していることを示しました。これらの研究により、性状がほとんど不明だった新奇ウイルスのタンパク質機能と植物内感染環の一端を解き明かすことに成功しました。
(1) Ishikawa K, Maejima K, Nagashima S, Sawamura N, Takinami Y, Komatsu K, Hashimoto M, Yamaji Y, Yamamoto J, Namba S: First report of fig mosaic virus infecting common fig (Ficus carica) in Japan. Gen. Plant Pathol. 78(2): 136-139. (2012)
(2) Ishikawa K, Maejima K, Netsu O, Fukuoka M, Nijo T, Hashimoto M, Takata D, Yamaji Y, Namba S: Rapid detection of fig mosaic virus using reverse transcription loop-mediated isothermal amplification. Gen. Plant Pathol. 81(5): 382-389. (2015)
(3) Ishikawa K, Maejima K, Komatsu K, Netsu O, Keima T, Shiraishi T, Okano Y, Hashimoto M, Yamaji Y, Namba S: Fig mosaic emaravirus p4 protein is involved in cell-to-cell movement. Gen. Virol. 94(3): 682-686. (2013)
(4) Ishikawa K, Hashimoto M, Yusa A, Koinuma H, Kitazawa Y, Netsu O, Yamaji Y, Namba S: Dual targeting of a virus movement protein to ER and plasma membrane subdomains is essential for plasmodesmata localization. PLoS Pathog. 13(6): e1006463. (2017)
小胞体-細胞膜接着部位の細胞内分布の解析と構成因子の同定
植物ウイルスの細胞内感染環の研究を通じて、植物細胞における小胞体-細胞膜接着部位の基本的性状が未解明であると感じたため、細胞内分布および構成因子を調査しました。上述した細胞膜への小胞体の係留に関与するとされるSYT1の細胞内局在を高い解像度で解析し、SYT1が小胞体と細胞膜の間に局在し物理的に両者のオルガネラ膜を繋いでいることを3次元的に初めて示しました。さらに、カルシウムイオン濃度依存的に小胞体-細胞膜の接着面積が変化することを発見しました。SYT1欠失変異体シロイヌナズナは野生型と比較して、浸透圧ストレスに感受性になることが知られていることから、環境ストレスのセカンドメッセンジャーであるカルシウムイオンに依存してSYT1が小胞体-細胞膜の接着面積を調節することで、小胞体-細胞膜間の物質輸送を制御し、浸透圧ストレスなどの環境ストレスに対応していると考えられました。次に、SYT1の相互作用因子について解析を行い、SYT1はSYT5およびSYT7と複合体を形成して小胞体と細胞膜の接着部位を構成していることを明らかにしました。これら3つの構成因子を全て欠いたシロイヌナズナ変異体は、通常条件での生育は野生型と差がないものの、細胞間をつなぐ構造体である原形質連絡の構造が変化しており、原形質連絡を貫通する小胞体(デスモチューブル)の狭窄が弱いことがわかりました。この変異体にウイルスを接種すると、ウイルス細胞間移動速度が野生型より遅延し、ウイルス感染に対し抵抗性となるという現象が見られました。このことから、小胞体-細胞膜接着部位は原形質連絡のデスモチューブルの狭窄形成に関与しており、狭窄領域を利用して植物ウイルスは細胞間移行を達成していることが明らかになりました。これらの研究から、ほとんど不明だった植物細胞の小胞体-細胞膜接着部位について、構成因子を明らかにし、病原との相互作用メカニズムの一部を明らかにすることに成功しました。

(1) Ishikawa K, Tamura K, Ueda H, Ito Y, Nakano A, Hara-Nishimura I, Shimada T: Synaptotagmin-associated endoplasmic reticulum-plasma membrane contact sites are localized to immobile ER tubules. Plant Physiol. 178(2): 641-653. (2018)
(2) Ishikawa K, Tamura K, Shimada T: Subcellular localisation of an endoplasmic reticulum-plasma membrane tethering factor, SYNAPTOTAGMIN 1, is affected by fluorescent protein fusion. Plant Signal. Behav. 13(12): e1547577. (2018)
(3) Ishikawa K, Tamura K, Fukao Y, Shimada T: Structural and functional relationships between plasmodesmata and plant endoplasmic reticulum–plasma membrane contact sites consisting of three synaptotagmins. New Phytol. 226(3): 798-808. (2020)
今後の研究
これまで石川助教は植物病の新規防除法を確立すべく、植物病原と植物細胞をそれぞれ研究してきました。しかし、植物病原は多様であり、広範囲の病原に対する普遍的な防除法の確立は難しいのが現状です。分子生物学分野は細菌学と免疫学を専門としている研究室であり、動物病原細菌の病原性やストレス耐性システム、免疫による宿主の病原排除システムについて、専門的な研究を行っています。病原と宿主の応答は動植物で共通する点が存在することから、動物病原とされる細菌に対する植物の応答や、反対に植物病原とされる細菌の動物免疫の応答を研究することで、生物に共通した普遍的な病原の感染メカニズムや病原に対する抵抗性のメカニズムを解き明かすことができるのではないかと考えています。また、ヒトの食中毒の原因細菌も、環境中では植物やその周辺の土壌に定着しており、食事などの経口接種を介してヒトに取り込まれることが知られています。このことから、一般に動物病原とされる細菌についても、植物との相互作用を研究することは公衆衛生上重要であると考えられます。しかし、これまでの研究の大半は、細菌が病原性を発揮する動物宿主に着目して研究を進めており、植物との関係を解析した研究はほとんどありません。以上の重要性から、石川助教はこれまでの研究内容と、本研究室の専門分野を活かし、動物病原とされる細菌と植物の相互作用や、植物病原とされる細菌と免疫応答の関係を研究して行こうと考えています。
