研究
research
薬学部が開拓する新世界
生体内ガスの生理的/病態生理的役割を薬理学的に明らかにして、新薬開発への応用を目指す!
教授 上原 孝
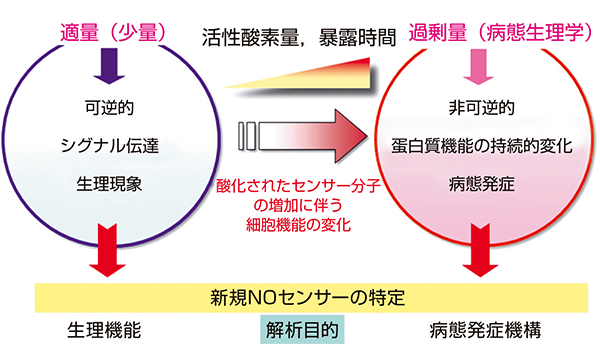
 私たちの体内ではガス状分子が酸化反応を介して生体機能を絶妙にコントロールしていることをご存知でしょうか?例えば、血圧調節や記憶形成には一酸化窒素が、バクテリアなどの外来生物侵入時には活性酸素が、酵素によって産生されます。最近では、社会問題にもなっている硫化水素も体内で酵素から合目的に適量だけ産生され、重要な働きを担っていることが報告されつつあります。これらの産生は通常は巧妙に制御されているのですが、このシステムが破綻して過剰量産生してしまうことがあります。このような状況下では生体(臓器)に酸化ストレスが負荷されています。これが疾患発症を招く原因の一つと推定されています。私の研究室ではこの酸化ストレスが脳の中でどのように発生して作用しているのかを詳しく研究しています。 薬理学という学問の特徴の一つとして、病態発症メカニズムの解明があります。病態ではどこに異常があるのかを分子(タンパク質、脂質、核酸など)レベルで調べ、それを細胞やモデル動物あるいは遺伝子改変動物を用いて証明します。最終的に、そこに薬を作用させて本当に効果があるのかどうかを調べます。薬を作るには、まず初めに病気を知ることが何よりも大切です。その情報を駆使して、新薬の種を見つけ、それを評価することこそ薬理学の真髄なのです。 科学が進歩した現在では、疾患発症メカニズム(情報)を基にして、異常部位にだけ作用するような薬を化合物ライブラリーから、あるいはコンピューター解析から単離することが出来るようになりました。また、最近話題の抗体医薬に関しても、遺伝子改変技術を駆使して特異的に作用する人工抗体を単離することが可能になりました。このような取り組みは、アルツハイマー病のような原因の未だ不明な難治性疾患に対する新薬を開発する上で貴重な情報をもたすであろうと期待されています。 当研究室の教員は、これまでに神経変性疾患(アルツハイマー病など)発症に関わる酸化ストレスの標的やアミロイドβ産生制御機構を発見し、世界で最も権威のあるジャーナルでその成果を発表してきました。今後も引き続き精力的な研究を行って、神経変性疾患をはじめとする病態の解明と抗酸化的な予防対策・治療戦略の確立に迫っていこうと考えています。
私たちの体内ではガス状分子が酸化反応を介して生体機能を絶妙にコントロールしていることをご存知でしょうか?例えば、血圧調節や記憶形成には一酸化窒素が、バクテリアなどの外来生物侵入時には活性酸素が、酵素によって産生されます。最近では、社会問題にもなっている硫化水素も体内で酵素から合目的に適量だけ産生され、重要な働きを担っていることが報告されつつあります。これらの産生は通常は巧妙に制御されているのですが、このシステムが破綻して過剰量産生してしまうことがあります。このような状況下では生体(臓器)に酸化ストレスが負荷されています。これが疾患発症を招く原因の一つと推定されています。私の研究室ではこの酸化ストレスが脳の中でどのように発生して作用しているのかを詳しく研究しています。 薬理学という学問の特徴の一つとして、病態発症メカニズムの解明があります。病態ではどこに異常があるのかを分子(タンパク質、脂質、核酸など)レベルで調べ、それを細胞やモデル動物あるいは遺伝子改変動物を用いて証明します。最終的に、そこに薬を作用させて本当に効果があるのかどうかを調べます。薬を作るには、まず初めに病気を知ることが何よりも大切です。その情報を駆使して、新薬の種を見つけ、それを評価することこそ薬理学の真髄なのです。 科学が進歩した現在では、疾患発症メカニズム(情報)を基にして、異常部位にだけ作用するような薬を化合物ライブラリーから、あるいはコンピューター解析から単離することが出来るようになりました。また、最近話題の抗体医薬に関しても、遺伝子改変技術を駆使して特異的に作用する人工抗体を単離することが可能になりました。このような取り組みは、アルツハイマー病のような原因の未だ不明な難治性疾患に対する新薬を開発する上で貴重な情報をもたすであろうと期待されています。 当研究室の教員は、これまでに神経変性疾患(アルツハイマー病など)発症に関わる酸化ストレスの標的やアミロイドβ産生制御機構を発見し、世界で最も権威のあるジャーナルでその成果を発表してきました。今後も引き続き精力的な研究を行って、神経変性疾患をはじめとする病態の解明と抗酸化的な予防対策・治療戦略の確立に迫っていこうと考えています。
新しい評価系を利用して、細菌の病原性を理解する
教授 垣内 力
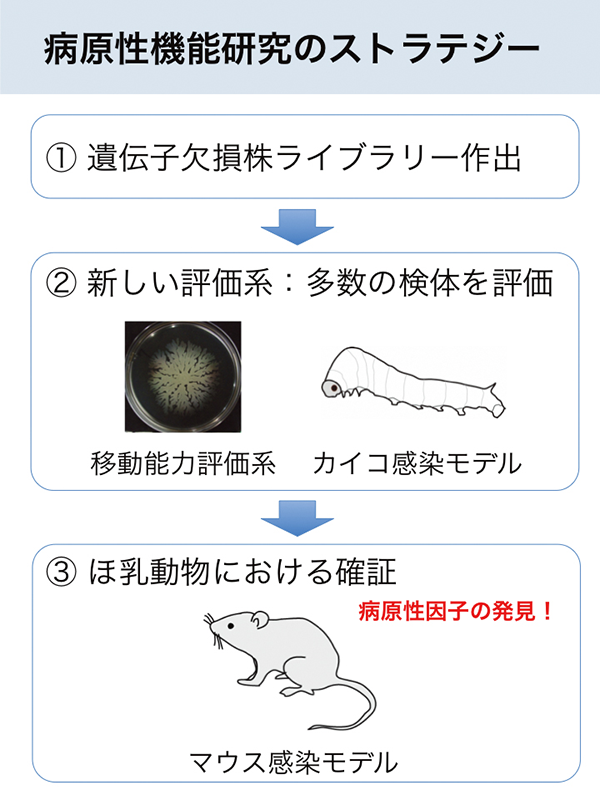
 病原性細菌は動物の体内に侵入し、その動物の栄養を奪うことにより増殖することができます。動物は細菌に対する精巧な防御システムを作り上げているにもかかわらず、時にはたった1個の細菌に侵入され、殺されてしまうこともあります。一方、動物の体には病原性を持たない常在細菌が数多く存在しています。細菌が動物に対して病原性を示すか、示さないかは、どうやって決まっているのでしょうか? これが、私たちが取り組んでいる研究テーマです。 細菌が病原性を示す分子メカニズムを理解するためには、病原性に関わる細菌因子を多数同定し、その機能を明らかにすることが必要です。しかしながら、これまで感染モデル動物として用いられてきたマウスなどのほ乳動物は倫理的な観点とコスト面から多数回の感染実験を行うことが困難であり、病原性因子の網羅的同定には適していませんでした。私は、この問題点を克服するために、細菌の病原性を評価する新しい系として、昆虫であるカイコを利用した感染モデルと細菌の移動能力の評価系を構築しました。これらの評価系を用いることにより、病原性制御機能を持つ細菌RNAや細菌の病原性を抑制する宿主タンパク質など、新しい病原性制御因子を解明することに成功しています。 地球上に存在する全ての動植物について、病原性細菌や常在細菌が存在することを考えると、細菌と宿主の相互作用の解明は地球上の生命を理解するために欠くことができません。また、その知見は薬学分野において、薬剤耐性菌に対する新しい治療薬創出を可能とします。学生、スタッフと協力し、生物間相互作用の基本原理の探求を通して創薬に貢献する研究を推進していく所存です。
病原性細菌は動物の体内に侵入し、その動物の栄養を奪うことにより増殖することができます。動物は細菌に対する精巧な防御システムを作り上げているにもかかわらず、時にはたった1個の細菌に侵入され、殺されてしまうこともあります。一方、動物の体には病原性を持たない常在細菌が数多く存在しています。細菌が動物に対して病原性を示すか、示さないかは、どうやって決まっているのでしょうか? これが、私たちが取り組んでいる研究テーマです。 細菌が病原性を示す分子メカニズムを理解するためには、病原性に関わる細菌因子を多数同定し、その機能を明らかにすることが必要です。しかしながら、これまで感染モデル動物として用いられてきたマウスなどのほ乳動物は倫理的な観点とコスト面から多数回の感染実験を行うことが困難であり、病原性因子の網羅的同定には適していませんでした。私は、この問題点を克服するために、細菌の病原性を評価する新しい系として、昆虫であるカイコを利用した感染モデルと細菌の移動能力の評価系を構築しました。これらの評価系を用いることにより、病原性制御機能を持つ細菌RNAや細菌の病原性を抑制する宿主タンパク質など、新しい病原性制御因子を解明することに成功しています。 地球上に存在する全ての動植物について、病原性細菌や常在細菌が存在することを考えると、細菌と宿主の相互作用の解明は地球上の生命を理解するために欠くことができません。また、その知見は薬学分野において、薬剤耐性菌に対する新しい治療薬創出を可能とします。学生、スタッフと協力し、生物間相互作用の基本原理の探求を通して創薬に貢献する研究を推進していく所存です。
『光』を薬にする研究!?
教授 須藤 雄気
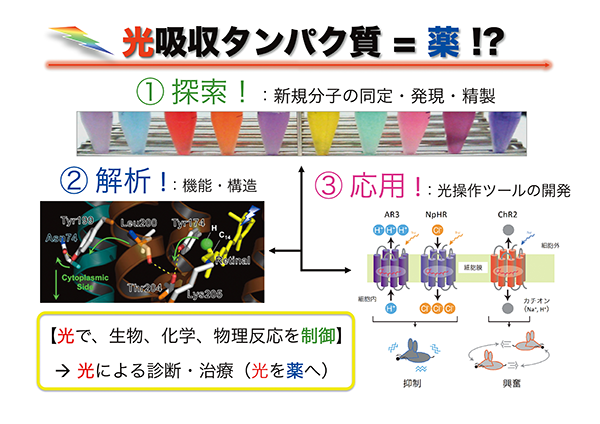
 みなさんは、『薬』と聞いて何を思い浮かべるでしょうか?炭素や窒素、酸素などからなる有機化合物でしょうか?あるいは抗体医薬品でしょうか?私たちの研究室では、『光』を薬にすることを目指した基礎研究を行っています。 様々な生物は、『光』を感じて生活しています。みなさんも、海岸線から昇る朝日で目を覚まし、国道沿いに咲き誇る草花にみとれながら学校(職場)に向かい、部活(職場)帰りに見える夕日に明日への希望を感じ、夜空に打ち上がる花火の美しさに感動した経験があるでしょう。このような時に、光をキャッチするのは、“レチナールタンパク質”と呼ばれる分子です。 私たちの研究室では、レチナールタンパク質について、①探索、②解析、③応用の3つの観点から、研究を行っています。これまでに、【①探索】様々な新規分子を発見するとともに、【②解析】レチナールタンパク質の機能が、エネルギー産生、情報伝達、転写調節など多岐にわたることを明らかにしてきました。すなわち、レチナールタンパク質を人為的に生物に発現させたり、運び屋分子に組み込んで生物中に取り込ませることで、生体内の生物、化学、物理応答を光で制御できるようになると考えられます。実際に、【③応用】光でイオンの流れを制御するレチナールタンパク質を取り込ませ、光による行動抑制に成功しています。 光は非侵襲的かつ可逆的な刺激であり、高い時間・空間領域での制御が可能です。私たちは、胃カメラの代わりに光ファイバーを飲んだり、レントゲンの代わりに光照射装置に入ったり、薬の代わりに発光ダイオード(LED)が処方されるような、『光』の時代を実現すべく、日々精進しています。
みなさんは、『薬』と聞いて何を思い浮かべるでしょうか?炭素や窒素、酸素などからなる有機化合物でしょうか?あるいは抗体医薬品でしょうか?私たちの研究室では、『光』を薬にすることを目指した基礎研究を行っています。 様々な生物は、『光』を感じて生活しています。みなさんも、海岸線から昇る朝日で目を覚まし、国道沿いに咲き誇る草花にみとれながら学校(職場)に向かい、部活(職場)帰りに見える夕日に明日への希望を感じ、夜空に打ち上がる花火の美しさに感動した経験があるでしょう。このような時に、光をキャッチするのは、“レチナールタンパク質”と呼ばれる分子です。 私たちの研究室では、レチナールタンパク質について、①探索、②解析、③応用の3つの観点から、研究を行っています。これまでに、【①探索】様々な新規分子を発見するとともに、【②解析】レチナールタンパク質の機能が、エネルギー産生、情報伝達、転写調節など多岐にわたることを明らかにしてきました。すなわち、レチナールタンパク質を人為的に生物に発現させたり、運び屋分子に組み込んで生物中に取り込ませることで、生体内の生物、化学、物理応答を光で制御できるようになると考えられます。実際に、【③応用】光でイオンの流れを制御するレチナールタンパク質を取り込ませ、光による行動抑制に成功しています。 光は非侵襲的かつ可逆的な刺激であり、高い時間・空間領域での制御が可能です。私たちは、胃カメラの代わりに光ファイバーを飲んだり、レントゲンの代わりに光照射装置に入ったり、薬の代わりに発光ダイオード(LED)が処方されるような、『光』の時代を実現すべく、日々精進しています。
化学合成によって自然界と創薬を繋ぐ
教授 好光 健彦
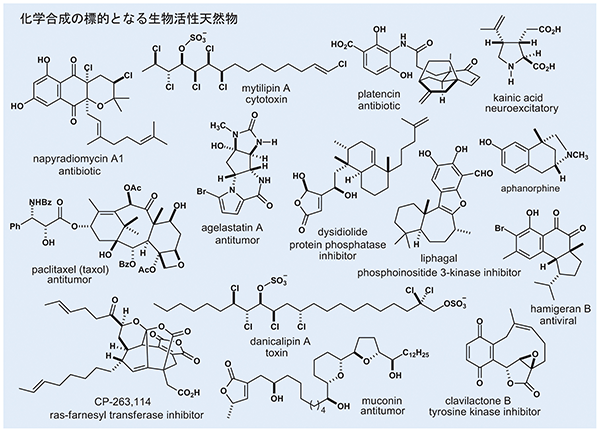
 我々人類は、自然界に見出される生物活性天然物を貴重な医薬資源として利用してきました。こうした天然物の多くが有機化合物であることから、その創製の礎となる有機合成化学の発展は創薬の歴史を支えてきたといえるでしょう。 我々は、有機化合物の新しい合成方法の開発に関する研究と、生物活性天然物の全合成(化学合成により人工的につくること)に基づく創薬研究を展開しています。生物活性天然物の全合成は、一原子単位で分子を組み上げる化学技術を駆使した物質創製に関わる科学であり、天然物をモチーフとして、自然界には存在しない物質を設計・合成し、価値ある医薬資源を我々の手で生み出すことにも繋がります。例えば、我々は、複雑で新奇な構造を特徴とするアルカロイド、テルペノイド、クロロスルホリピッドを含むさまざまな生物活性天然物の全合成を達成し、これをもとに国内外の研究者と協力して創薬・生命科学研究を進めてきました。その結果、海洋産抗腫瘍活性天然物アゲラスタチンが脳腫瘍や心疾患の創薬に新たな可能性を拓くことや、脂肪酸合成酵素阻害活性天然物プラテンシンが多剤耐性結核菌の増殖を顕著に阻害することなどを明らかにしています。 こうした有機化合物の合成において、我々が特に着目しているのが、非常に強力且つ多彩な反応性を示すフリーラジカルによる化学反応です。我々は独自に開発したラジカル反応を活用することによって、これまでの方法では困難であった天然物の人工合成にも成功しています。 自然界に存在する天然物はもとより、我々の体内で働く生体分子など、あらゆる有機化合物の機能がその化学構造によって制御されていることから、化学構造を自在につくり、改変できる有機合成化学への期待が今後益々高まるでしょう。我々はこの化学を洗練する匠となり、役立つ物質を生み出すことで世界に貢献すべく研究を推進しています。
我々人類は、自然界に見出される生物活性天然物を貴重な医薬資源として利用してきました。こうした天然物の多くが有機化合物であることから、その創製の礎となる有機合成化学の発展は創薬の歴史を支えてきたといえるでしょう。 我々は、有機化合物の新しい合成方法の開発に関する研究と、生物活性天然物の全合成(化学合成により人工的につくること)に基づく創薬研究を展開しています。生物活性天然物の全合成は、一原子単位で分子を組み上げる化学技術を駆使した物質創製に関わる科学であり、天然物をモチーフとして、自然界には存在しない物質を設計・合成し、価値ある医薬資源を我々の手で生み出すことにも繋がります。例えば、我々は、複雑で新奇な構造を特徴とするアルカロイド、テルペノイド、クロロスルホリピッドを含むさまざまな生物活性天然物の全合成を達成し、これをもとに国内外の研究者と協力して創薬・生命科学研究を進めてきました。その結果、海洋産抗腫瘍活性天然物アゲラスタチンが脳腫瘍や心疾患の創薬に新たな可能性を拓くことや、脂肪酸合成酵素阻害活性天然物プラテンシンが多剤耐性結核菌の増殖を顕著に阻害することなどを明らかにしています。 こうした有機化合物の合成において、我々が特に着目しているのが、非常に強力且つ多彩な反応性を示すフリーラジカルによる化学反応です。我々は独自に開発したラジカル反応を活用することによって、これまでの方法では困難であった天然物の人工合成にも成功しています。 自然界に存在する天然物はもとより、我々の体内で働く生体分子など、あらゆる有機化合物の機能がその化学構造によって制御されていることから、化学構造を自在につくり、改変できる有機合成化学への期待が今後益々高まるでしょう。我々はこの化学を洗練する匠となり、役立つ物質を生み出すことで世界に貢献すべく研究を推進しています。
遺伝情報を有する核酸を化学し薬を創る!
教授 谷口 陽祐
 遺伝情報を蓄えているDNAやそれを伝えるRNAを構成している核酸(ヌクレオシド)が連なったオリゴヌクレオチドは、これまでにない新しい「くすり」になるため注目を集めています。核酸創成化学研究室では、核酸の構造を独自に変更した人工核酸を化学合成しています。そして、それら人工核酸を用いて、遺伝子発現を人工的にコントロール可能な手法へ展開し、ガンなどの遺伝子の異常を伴う疾患の新たな治療薬、「核酸医薬」の開発を行っています。また、遺伝子のキズといわれている部分を見つけ出す人工核酸の開発も行っており、それらキズと疾患の関係を明らかにする「核酸診断薬」の開発も行うべく、日々研究に取り組んでいます。
遺伝情報を蓄えているDNAやそれを伝えるRNAを構成している核酸(ヌクレオシド)が連なったオリゴヌクレオチドは、これまでにない新しい「くすり」になるため注目を集めています。核酸創成化学研究室では、核酸の構造を独自に変更した人工核酸を化学合成しています。そして、それら人工核酸を用いて、遺伝子発現を人工的にコントロール可能な手法へ展開し、ガンなどの遺伝子の異常を伴う疾患の新たな治療薬、「核酸医薬」の開発を行っています。また、遺伝子のキズといわれている部分を見つけ出す人工核酸の開発も行っており、それらキズと疾患の関係を明らかにする「核酸診断薬」の開発も行うべく、日々研究に取り組んでいます。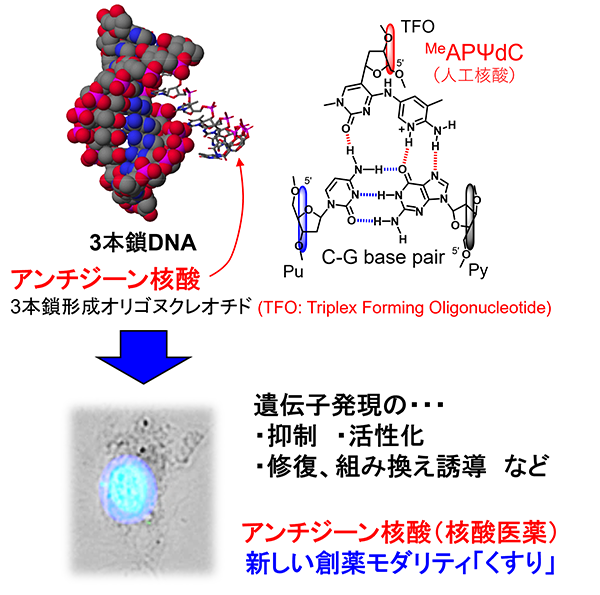
『医療ビッグデータ』で新たな価値を生み出す!
教授 小山 敏広
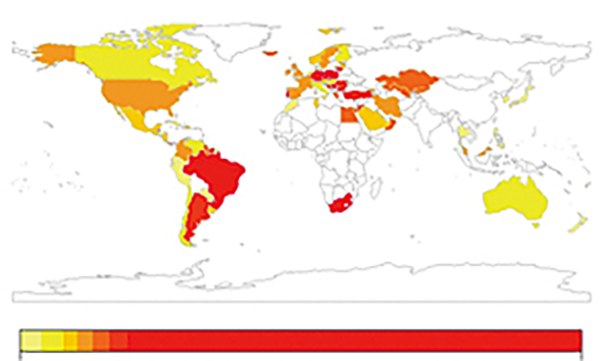
 “ビッグデータ”についてはみなさんどんなイメージをもっていますか。SNSやインターネットの膨大な情報をイメージするかもしれませんね。医療におけるビッグデータには、様々な病気において、どれくらいの患者さんが困っていて、どのような治療が行われ、その結果はどうであったのか、数千種類にも及ぶ多様なデータが含まれています。今、これらの膨大な医療ビッグデータを活用した研究が国境なく世界中で加速しています。2010年以降研究成果は増え続け新たな価値を提供し続けています。 医療ビッグデータの活用には様々な利点があります。これまでわずかな医療施設でしか行えなかった臨床研究に対し、医療ビッグデータはすべての医療施設を対象にした研究も実施可能にします。さらに、安全に薬を使うために欠かせない副反応に関する情報も一例ずつ集める代わりにすべての患者さんを対象に調査することが可能になり、まれな副反応も正確に把握できるようになりつつあります。このように、これまで知りえなかった研究成果は、多くの患者さんや医療者が困っている問題に対して新しいアプローチによる解決策を提示することを可能にしています。 医療ビッグデータの活用には、疫学、生物統計学、情報学などの複合的な技術に加え、薬学の知識と実際の患者さんや医療者との対話から得る臨床経験に基づく視点が欠かせません。 現在、私は日本と米国の研究者と主に、様々な医療ビッグデータの活用に協働して取り組んでいます。図に示したのは世界約100か国を対象に特定の循環器疾患による死亡率を国毎にマッピングした結果です。このような国際的な医療の動向を詳細に分析することも医療ビッグデータが得意とする分野の一つです。 薬学部では、病気や薬の効果における生命科学を学ぶことができ、さらに医療施設における実習によって臨床感覚を身に着けることもできます。 今後一層、医療ビッグデータの活用を進め、多くのみなさんと共に新たな価値を患者さんにお届けしたいと思います。
“ビッグデータ”についてはみなさんどんなイメージをもっていますか。SNSやインターネットの膨大な情報をイメージするかもしれませんね。医療におけるビッグデータには、様々な病気において、どれくらいの患者さんが困っていて、どのような治療が行われ、その結果はどうであったのか、数千種類にも及ぶ多様なデータが含まれています。今、これらの膨大な医療ビッグデータを活用した研究が国境なく世界中で加速しています。2010年以降研究成果は増え続け新たな価値を提供し続けています。 医療ビッグデータの活用には様々な利点があります。これまでわずかな医療施設でしか行えなかった臨床研究に対し、医療ビッグデータはすべての医療施設を対象にした研究も実施可能にします。さらに、安全に薬を使うために欠かせない副反応に関する情報も一例ずつ集める代わりにすべての患者さんを対象に調査することが可能になり、まれな副反応も正確に把握できるようになりつつあります。このように、これまで知りえなかった研究成果は、多くの患者さんや医療者が困っている問題に対して新しいアプローチによる解決策を提示することを可能にしています。 医療ビッグデータの活用には、疫学、生物統計学、情報学などの複合的な技術に加え、薬学の知識と実際の患者さんや医療者との対話から得る臨床経験に基づく視点が欠かせません。 現在、私は日本と米国の研究者と主に、様々な医療ビッグデータの活用に協働して取り組んでいます。図に示したのは世界約100か国を対象に特定の循環器疾患による死亡率を国毎にマッピングした結果です。このような国際的な医療の動向を詳細に分析することも医療ビッグデータが得意とする分野の一つです。 薬学部では、病気や薬の効果における生命科学を学ぶことができ、さらに医療施設における実習によって臨床感覚を身に着けることもできます。 今後一層、医療ビッグデータの活用を進め、多くのみなさんと共に新たな価値を患者さんにお届けしたいと思います。
再生治療薬学で難治性疾患を克服する
教授 堀口 道子
 これまで治療が困難であった難治性疾患に対して、失われた組織や臓器を再生させる再生治療が注目されています。しかし、再生治療を実現する幹細胞などの再生治療の製品は品質が不安定かつ高額なため普及の障害となっています。そのため、品質の安定した高い治療効果を持つ安価な幹細胞製剤の開発は急務の課題となっています。当研究室では、安定して高い幹細胞性を保つ分子機構を解明し、新しい幹細胞製剤の開発に取り組んでいます。
これまで治療が困難であった難治性疾患に対して、失われた組織や臓器を再生させる再生治療が注目されています。しかし、再生治療を実現する幹細胞などの再生治療の製品は品質が不安定かつ高額なため普及の障害となっています。そのため、品質の安定した高い治療効果を持つ安価な幹細胞製剤の開発は急務の課題となっています。当研究室では、安定して高い幹細胞性を保つ分子機構を解明し、新しい幹細胞製剤の開発に取り組んでいます。
1. 次世代がん治療に向けて幹細胞の遺伝子安定性とがん化の関連を解明
幹細胞の中でも様々な細胞に分化することのできる万能性幹細胞(ES細胞)と人工多能性幹細胞(iPS細胞)を研究対象として、幹細胞の遺伝子修復に不可欠なタンパク質を特定することに成功し、がん化のメカニズムを解明しました。この研究を、再生治療における幹細胞のがん化の抑制や、幹細胞を標的としたがんの遺伝子治療やがん予防に繋げるべく研究を継続しています。
2.再生治療の普及に向けて幹細胞の機能を解明
幹細胞の特徴を明らかにし、基礎疾患の有無により幹細胞の特性の違いを明らかにすることは、再生治療の効率を高めることに繋がります。私達は、糖尿病患者由来の幹細胞においてミトコンドリアや核膜の変性が起こることを明らかにしました。さらに、幹細胞移植後の移植効率に影響を及ぼす時計遺伝子の日内変動を明らかにすることに成功しました。幹細胞の特徴や機能を明らかにすることで、幹細胞の品質評価の方法や保存方法の確立に繋げていきます。
3.高い再生治療効果の実現に向けて幹細胞移植効率を決定する因子を解明
高い再生治療効果を実現するために、幹細胞移植の効率を決定する因子として、4つの遺伝子を発見しました。これらの遺伝子を制御すると、移植効率を改善させることができ、効果の高い再生治療の実現に繋がります。
これらの研究成果を生かして、当研究室では幹細胞製剤の開発に取り組んでいます。これからも、病気の根本にアプローチし、効率的に治療が可能な薬学の技術を再生治療の分野に取り入れ、治療法のない病気をなくせるように研究室一丸となって取り組んで参ります。
ゲノム編集技術を駆使したがん治療戦略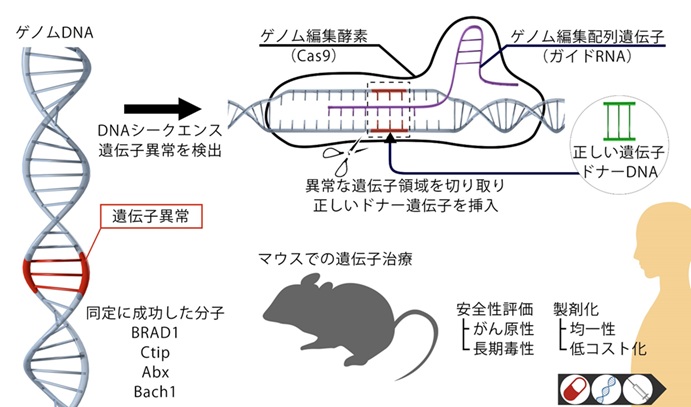
新たなコンセプトで、てんかん治療薬の開発に挑む
准教授 井上 剛
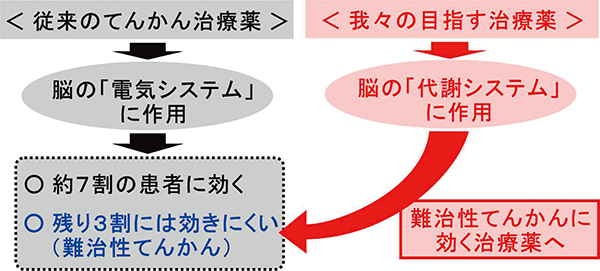
 脳では、多くの脳細胞が「電気信号」をやりとりしながら働いています。我々が物を考えたり、運動ができるのは、脳で電気が流れているからです。しかし、脳細胞の電気活動が過剰になると、「てんかん」という病気になります。 全人口の約1%がてんかんを患っています。しかもその約3割の患者は、現在使われている治療薬でコントロールできません。新しい治療薬が必要です。興味深いことに、この薬が効かない「難治性てんかん」に対し、ケトン食療法(1920年代に確立した食事療法の1つ)が効きます。つまり、ケトン食療法には、現在の治療薬にはない未知の仕組みがあるはずです。そして、これを明らかにすれば100年来の治療薬誕生の道が拓けます。 我々はその仕組みを明らかにしました。ケトン食療法によるてんかん抑制には、脳のグリア細胞から神経細胞へ「乳酸」という物質を運ぶ代謝経路が重要であることを見出しました。さらに、この代謝経路をどのようにコントロールすれば、てんかん治療薬を作ることができるのか、具体的な道筋を示すこともできました。これは、岡山大学の大学院生による研究成果です (Sada et al, Science, 2015)。 従来のてんかん治療薬開発は、脳の電気活動を直接制御するよう進められてきました。てんかんが、脳の過剰な電気活動で引き起こされるためです。しかし、我々の研究により、あえて脳の電気システムを狙わず、代謝システムを狙った創薬も可能であることが分かりました。てんかんで苦しむ患者さんのために、代謝システムに作用する画期的治療薬 (first-in-class) を開発すべく、一歩ずつ前進していきたいと考えています。
脳では、多くの脳細胞が「電気信号」をやりとりしながら働いています。我々が物を考えたり、運動ができるのは、脳で電気が流れているからです。しかし、脳細胞の電気活動が過剰になると、「てんかん」という病気になります。 全人口の約1%がてんかんを患っています。しかもその約3割の患者は、現在使われている治療薬でコントロールできません。新しい治療薬が必要です。興味深いことに、この薬が効かない「難治性てんかん」に対し、ケトン食療法(1920年代に確立した食事療法の1つ)が効きます。つまり、ケトン食療法には、現在の治療薬にはない未知の仕組みがあるはずです。そして、これを明らかにすれば100年来の治療薬誕生の道が拓けます。 我々はその仕組みを明らかにしました。ケトン食療法によるてんかん抑制には、脳のグリア細胞から神経細胞へ「乳酸」という物質を運ぶ代謝経路が重要であることを見出しました。さらに、この代謝経路をどのようにコントロールすれば、てんかん治療薬を作ることができるのか、具体的な道筋を示すこともできました。これは、岡山大学の大学院生による研究成果です (Sada et al, Science, 2015)。 従来のてんかん治療薬開発は、脳の電気活動を直接制御するよう進められてきました。てんかんが、脳の過剰な電気活動で引き起こされるためです。しかし、我々の研究により、あえて脳の電気システムを狙わず、代謝システムを狙った創薬も可能であることが分かりました。てんかんで苦しむ患者さんのために、代謝システムに作用する画期的治療薬 (first-in-class) を開発すべく、一歩ずつ前進していきたいと考えています。
トランスポーターに着目した植物ストレス耐性研究の新展開
准教授 宮地 孝明
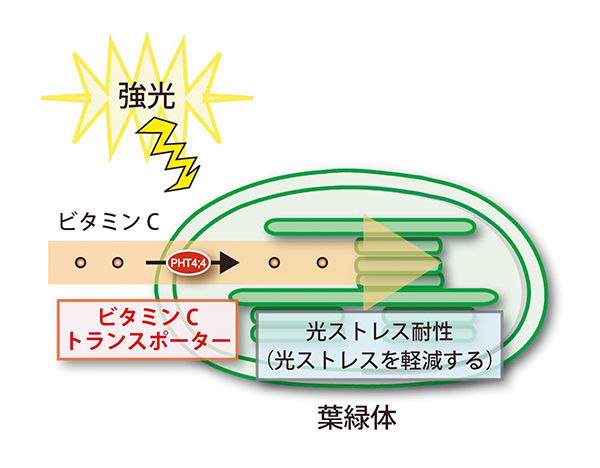
 植物は自ら動くことができないため、強光・乾燥・酸性土壌・病原体感染など多くの環境ストレスにさらされています。これらの環境ストレス下でも適応するために、植物はビタミンCやサリチル酸などのストレス耐性物質を自ら作り、ストレスを受けている場所に運び、環境ストレスを緩和しています。これらの物質を運ぶ膜タンパク質のことをストレス耐性物質トランスポーターと呼んでいます。このトランスポーターは環境ストレス耐性の仕組みに重要でありながら、その機能はほとんどわかっていませんでした。 私は、本学薬学部生体膜生化学研究室に在籍時にあらゆるトランスポーターを評価することができる方法を開発し、植物のストレス耐性物質トランスポーターの研究に取り組んできました。最近の研究成果としてビタミンCに着目したものがあります。ビタミンCはヒトに欠かすことができない微量栄養素の一つですが、植物においても前述のように、強光により葉緑体内に生じたストレスを緩和し、葉やけなどの光障害を防ぐ働きがあります。私たちは、独自に開発したトランスポーターの評価方法を用いて、植物の葉緑体の中にビタミンCを運ぶトランスポーターを発見しました。これは植物では初めてのビタミンCトランスポーターの発見であり、Nature Plants誌でも話題になりました。この研究の中で、このトランスポーター遺伝子が破壊された植物は、葉緑体内にビタミンCが運ばれなくなり、光ストレスを受けやすくなることを明らかにしました。 これらの成果から、葉緑体のビタミンC輸送を制御することで、光ストレス下に適応できるストレス耐性能を備えた植物育種への応用が期待できます。私たちは、薬用植物・作物の収量向上や地球の温暖化の解決に向けた緑化対策などに貢献したいと考えています。
植物は自ら動くことができないため、強光・乾燥・酸性土壌・病原体感染など多くの環境ストレスにさらされています。これらの環境ストレス下でも適応するために、植物はビタミンCやサリチル酸などのストレス耐性物質を自ら作り、ストレスを受けている場所に運び、環境ストレスを緩和しています。これらの物質を運ぶ膜タンパク質のことをストレス耐性物質トランスポーターと呼んでいます。このトランスポーターは環境ストレス耐性の仕組みに重要でありながら、その機能はほとんどわかっていませんでした。 私は、本学薬学部生体膜生化学研究室に在籍時にあらゆるトランスポーターを評価することができる方法を開発し、植物のストレス耐性物質トランスポーターの研究に取り組んできました。最近の研究成果としてビタミンCに着目したものがあります。ビタミンCはヒトに欠かすことができない微量栄養素の一つですが、植物においても前述のように、強光により葉緑体内に生じたストレスを緩和し、葉やけなどの光障害を防ぐ働きがあります。私たちは、独自に開発したトランスポーターの評価方法を用いて、植物の葉緑体の中にビタミンCを運ぶトランスポーターを発見しました。これは植物では初めてのビタミンCトランスポーターの発見であり、Nature Plants誌でも話題になりました。この研究の中で、このトランスポーター遺伝子が破壊された植物は、葉緑体内にビタミンCが運ばれなくなり、光ストレスを受けやすくなることを明らかにしました。 これらの成果から、葉緑体のビタミンC輸送を制御することで、光ストレス下に適応できるストレス耐性能を備えた植物育種への応用が期待できます。私たちは、薬用植物・作物の収量向上や地球の温暖化の解決に向けた緑化対策などに貢献したいと考えています。